Çoğu insan için ”radyasyon” kelimesi tehlike anlamına gelir. Ancak aslında hayatın her saniyesinde bazen doğal bazen de yapay radyasyona maruz kalıyoruz. Bu tehlike algısının temel nedeni bir çok kişinin radyasyon ile radyoaktiviteyi birbirine karıştırmasıdır. Peki ama radyasyon ve radyoaktivite tam olarak nedir?

Radyoaktivite ve radyasyon sıklıkla birbirinin yerine kullanılmaktadır. Ancak ilişkili olsa da özünde farklı süreçleri tanımlarlar. Ancak bu farklılığa girmeden önce atomların ne olduğunu ve nasıl davrandıklarıyla ilgili birkaç kavramı anlamakta fayda var.
Atom, kimyasal olarak tanımlanabilecek en küçük parçacıktır. Her atomun merkezinde çok sayıda proton (pozitif yüklü parçacıklar) içeren bir çekirdek vardır. Proton sayısı atomun hangi kimyasal olduğunu belirleyecektir.
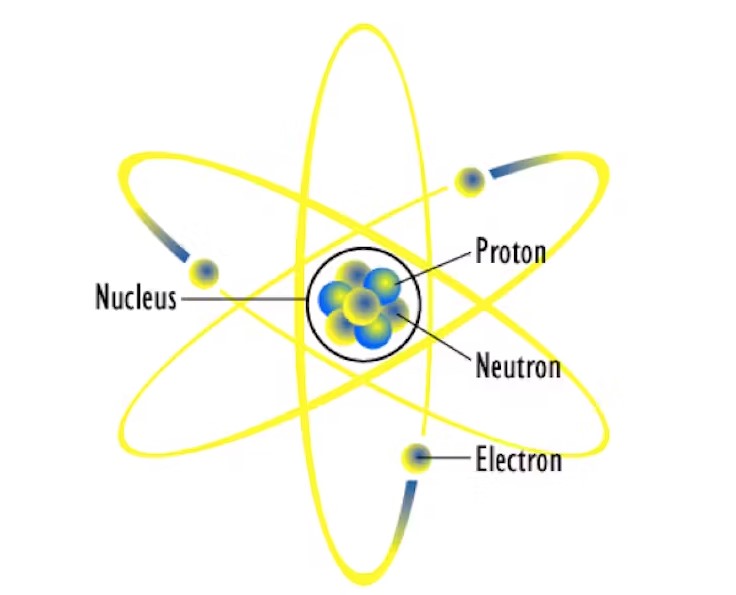
Örneğin tüm karbon çekirdekleri altı proton içerir. Beş proton bir bor atomu, yedi proton ise bir nitrojen atomu olacaktır. Çekirdek ayrıca bir dizi nötron (yüksüz parçacık) içermektedir. Aynı kimyasalın atomları farklı sayıda nötronlara sahip olabilir.
Örneğin karbon atomlarının yaklaşık %99’unda altı nötron vardır. Bu sayı altı protona eklendiğinde 12’lik bir atom kütlesi verir. Bazı karbon atomlarında daha fazla veya daha az nötron vardır. Bu durumda yedi nötron karbon-13’ü, sekiz nötron ise karbon-14’ü oluşturur. Karbon-12 ve karbon-13’ün çekirdekleri stabildir, ancak karbon-14 radyoaktiftir ve radyokarbon tarihlemesinin temelini oluşturur. Aynı kimyasalın farklı sayıda nötron içeren atomlarına izotoplar denir.
Çekirdeğin çevresinde elektron adı verilen çok küçük negatif yüklü parçacıklar bulunur. Bir atomda proton sayısı kadar elektron vardır. Atoma bir elektron eklenmesi veya atomdan bir elektronun çıkarılması, iyon adı verilen yüklü bir parçacığın oluşmasına neden olur. İyonlar atomlara çok farklı tepki verebilirler. Örneğin Klor atomu çok reaktif ve tehlikelidir ancak klorür iyonu sofra tuzunun bir parçasıdır.
Radyoaktivite Nedir?
Radyoaktivite, bir atom çekirdeğinin parçalanmasına (bozunmasına) veya yeniden düzenlenmesine verilen terimdir. Radyoaktif bozunma çeşitli şekillerde meydana gelir; en yaygın olanları şunlardır:

- Kendiliğinden fisyon: Yalnızca görece daha ağır kimyasal elementlerde görülen bir radyoaktif bozunma biçimidir. Çekirdeğin iki parçaya ayrılması nedeniyle “atomun bölünmesi” olarak da bilinmektedir.
- Nötron emisyonu: Fazla nötron içeren atomlarda gerçekleşen radyoaktif bir bozunma tepkimesidir. Bu bozunmada nötron basitçe çekirdekten atılacaktır.
- Alfa bozunması: Atomun alfa parçacığı saçarak fazla enerjisinden kurtulmasıdır. Alfa saçılması radyoaktif saçılmadır. Saçılma durumunda atom numarası 2, kütle numarası ise 4 azalır. Örneğin uranyum-238 alfa bozunması geçirerek toryum-234 elementine dönüşür.
- Beta bozunması: Beta bozunması, bir atom çekirdeğinden beta ışınının yayıldığı radyoaktif bir bozunmadır. Beta bozunması sırasında çekirdekteki proton nötrona dönüşür ve bunun tersi de geçerlidir. Protonun nötrona dönüşmesine β+ bozunması denir. Benzer şekilde, bir nötronun protona dönüşmesi β– bozunması olarak bilinmektedir.
- Gama bozunması: Çekirdek içindeki protonlar ve nötronlar daha kararlı bir biçime yeniden düzenlenecektir.
Yarı Ömür nedir?

Nötron emisyonu, alfa ve beta bozunmasının tümüne bir parçacığın salınması eşlik eder. Radyasyon temelinde bu parçacıktır. Her çekirdeğin belirli bir sürede kendiliğinden bozunma şansı 50/50’dir. Bir numunedeki atomların yarısının bozunması için geçen sürenin uzunluğuna “ yarı ömür ” denir.
Bir izotopun yarı ömrü, bu türdeki tüm çekirdekler için aynıdır. Örneğin tüm karbon-14 çekirdeklerinin yarı ömrü yaklaşık 5.750 yıl ve tüm karbon-15 çekirdeklerinin yarı ömrü yaklaşık 2,5 saniyedir. Bir malzemenin yarı ömrü uzunsa (örneğin uranyum-238’in 4,5 milyar yıllık yarı ömrü gibi) çok fazla radyoaktif değildir. Yarı ömrü kısa olan bir malzeme ( polonyum 210 – 138 gün) oldukça radyoaktiftir.
Radyoaktivite ve radyasyon arasındaki fark nedir?
Gördüğünüz gibi radyoaktivite temelinde çekirdek ile alakalıdır. Bu tepkimelere maruz kalarak parçalanan maddelere ‘radyoaktif madde’, çevreye yayılan alfa, beta ve gama gibi ışınlara ise ‘radyasyon’ adı verilmektedir. Bu radyasyon üç türe ayrılmaktadır. ( Ek okumalar için: Radyo Dalgalarından Gama Işınlarına: Elektromanyetik Dalgalar Nedir?)

İyonlaştırıcı olmayan radyasyon: İyonlaştırıcı olmayan radyasyon, bir atomdan veya molekülden bir elektronu tamamen koparabilmek için atomları veya molekülleri iyonlaştırabilecek yeterli enerjiye sahip olmayan herhangi bir elektromanyetik radyasyon türüdür. Bu, gördüğünüz tüm ışığı, radyo dalgalarını ve kızılötesi ışınları içerir.
İyonlaştırıcı radyasyon: Bir atomun yörüngesinden sıkı bir şekilde bağlı elektronları çıkaracak ve o atomun yüklenmesine veya iyonlaşmasına neden olacak yeterli enerjiye sahip radyasyondur. Doku içinden geçerken bıraktığı etki radyasyon ve kanser bağıntısının temelini oluşturmaktadır.
İyonlaştırıcı radyasyon iki ana forma ayrılır: Yüksek enerjili elektromanyetik radyasyon (X-ışını ve gama ışınları dahil) ve parçacık radyasyonu (alfa ve beta parçacıkları). İyonlaştırıcı radyasyonun bu farklı biçimleri, hasar verme kapasiteleri ve malzemelere nüfuz etme yetenekleri bakımından farklılık gösterir.
Nötronlar: diğer atomlarla çarpışabilen serbest nötron parçacıkları.

Radyoaktivite ve radyasyonun tüm bu biçimleri doğal olarak meydana gelir. Sonrasında da hep beraber Arka plan radyasyonu adı verilen şeyi oluştururlar. Yukarıdaki oranlardan da anlayacağınız gibi bu arka plan radyasyonun çoğunluğu doğal radyasyondur.

Sievert, radyasyon dozu birimi olarak kullanılan bir ölçü birimidir. Bir Sievert, dokuların radyasyona maruz kalmalarından kaynaklanan hasarın miktarını ölçmek için kullanılmaktadır.
Kaynaklar ve ileri okumalar:
- What is radioactivity?; Yayınlanma tarihi: 29 Ekim 1921; Bağlantı: https://cosmosmagazine.com/
- Explainer: the difference between radiation and radioactivity. Yayınlanma tarihi: 8 Ekim 2021. Bağlantı: Explainer: the difference between radiation and radioactivity
Matematiksel





